113838
论文已发表
注册即可获取德孚的最新动态
IF 收录期刊
- 3.4 Breast Cancer (Dove Med Press)
- 3.2 Clin Epidemiol
- 2.6 Cancer Manag Res
- 2.9 Infect Drug Resist
- 3.7 Clin Interv Aging
- 5.1 Drug Des Dev Ther
- 3.1 Int J Chronic Obstr
- 6.6 Int J Nanomed
- 2.6 Int J Women's Health
- 2.9 Neuropsych Dis Treat
- 2.8 OncoTargets Ther
- 2.0 Patient Prefer Adher
- 2.2 Ther Clin Risk Manag
- 2.5 J Pain Res
- 3.0 Diabet Metab Synd Ob
- 3.2 Psychol Res Behav Ma
- 3.4 Nat Sci Sleep
- 1.8 Pharmgenomics Pers Med
- 2.0 Risk Manag Healthc Policy
- 4.1 J Inflamm Res
- 2.0 Int J Gen Med
- 3.4 J Hepatocell Carcinoma
- 3.0 J Asthma Allergy
- 2.2 Clin Cosmet Investig Dermatol
- 2.4 J Multidiscip Healthc

比较体外 Fick’s 第一定律,体外脂解和体内大鼠模型基于 BCS II 类药物 SNEDDS 的口服吸收
Authors Ye J, Wu H, Huang C, Lin W, Zhang C, Huang B, Lu B, Xu H, Li X, Long X
Received 2 February 2019
Accepted for publication 17 June 2019
Published 23 July 2019 Volume 2019:14 Pages 5623—5636
DOI https://doi.org/10.2147/IJN.S203911
Checked for plagiarism Yes
Review by Single-blind
Peer reviewers approved by Dr Cristina Weinberg
Peer reviewer comments 2
Editor who approved publication: Dr Lei Yang
目的:基于生物药剂学分类系统(BCS)II 类药物的自纳米乳递药系统(SNEDDS)的口服吸收,比较体外 Fick’s 第一定律,体外脂解和体内大鼠方法,并研究药物性质及油的性质对药物吸收的影响。
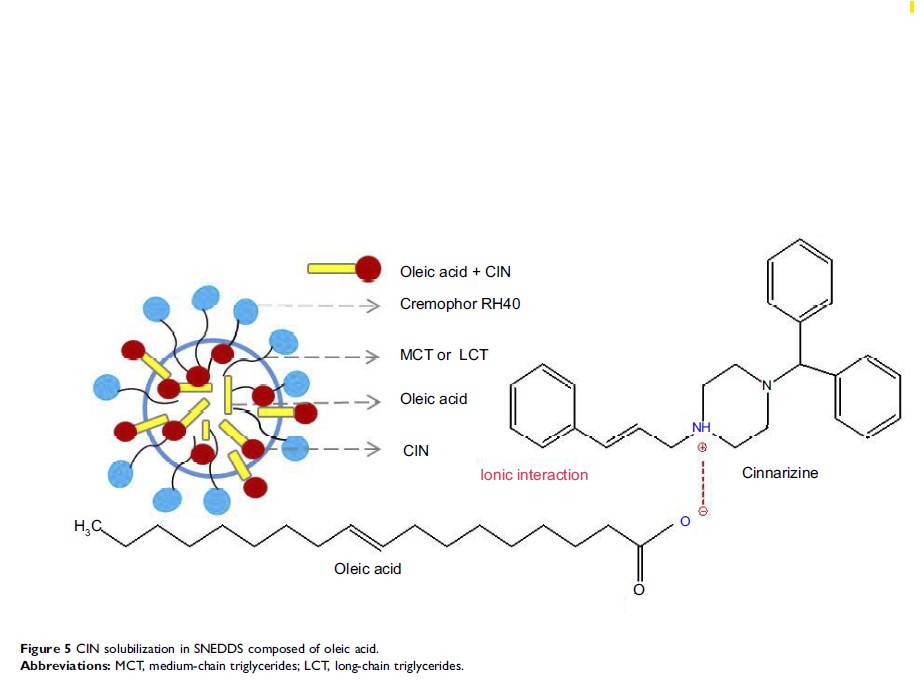
方法:利用体外犬(肾)上皮细胞(MCCK cell)模型研究灰黄霉素(GRI)、苯妥英(PHE)、吲哚美辛(IND)和酮洛芬(KET)的水饱和溶液及其 SNEDDS 的转运能力。GRI 的中链甘油三酯(MCT)-SNEDDS 和长链甘油三酯(LCT)-SNEDDS,桂利嗪(CIN)的 MCT-SNEDDS 和 LCT-SNEDDS,用于 SD 大鼠口服吸收和体外脂解模型以比较口服吸收及药物在胃肠道中分布行为的差异,并建立体内外相关性(IVIVC)。
结果:在细胞模型中,GRI、PHE、IND 和 KET 在 SNEDDS 中的溶解度相比饱和水溶液提高了 6~8 倍,但是其渗透性却仅分别为饱和水溶液的 18%、4%、8% 和 33%。然而,体内 GRI-SNEDDS 的口服吸收却是 GRI 混悬液的 2 倍,CIN-SNEDDS 是 CIN 混悬液的 15~21 倍。在体外脂解模型中,GRI 分布百分含量(GRI%)在 MCT 和 LCT-SNEDDS 的水相和沉淀相分布含量无差异。相比之下,CIN% 在水相和沉淀相中逐步降低并转移至脂质相。此外,脂质相中的 CIN% 与体内相对口服生物利用度(F r)具有一定的 IVIVC。
结论:体外细胞模型依然适合用于研究药物性质对转运能力的影响及 SNEDDS 吸收机制的研究。体外脂解模型相比细胞模型更适合用于模拟 SNEDDS 的口服吸收,并有助于建立与大鼠体内吸收的相关性。SNEDDS 中药物的性质及油的性质均能够影响药物的口服吸收。
关键词:自纳米乳递药系统,犬(肾)上皮细胞模型,体内大鼠模型,体外脂解,体内外相关性