113730
论文已发表
注册即可获取德孚的最新动态
IF 收录期刊
- 3.4 Breast Cancer (Dove Med Press)
- 3.2 Clin Epidemiol
- 2.6 Cancer Manag Res
- 2.9 Infect Drug Resist
- 3.7 Clin Interv Aging
- 5.1 Drug Des Dev Ther
- 3.1 Int J Chronic Obstr
- 6.6 Int J Nanomed
- 2.6 Int J Women's Health
- 2.9 Neuropsych Dis Treat
- 2.8 OncoTargets Ther
- 2.0 Patient Prefer Adher
- 2.2 Ther Clin Risk Manag
- 2.5 J Pain Res
- 3.0 Diabet Metab Synd Ob
- 3.2 Psychol Res Behav Ma
- 3.4 Nat Sci Sleep
- 1.8 Pharmgenomics Pers Med
- 2.0 Risk Manag Healthc Policy
- 4.1 J Inflamm Res
- 2.0 Int J Gen Med
- 3.4 J Hepatocell Carcinoma
- 3.0 J Asthma Allergy
- 2.2 Clin Cosmet Investig Dermatol
- 2.4 J Multidiscip Healthc

Atezolizumab 治疗肿瘤的安全性和有效性:系统评价和汇总分析
Authors Tie Y, Yang H, Zhao R, Zheng H, Yang D, Zhao J, Liu M
Received 27 September 2018
Accepted for publication 9 January 2019
Published 4 February 2019 Volume 2019:13 Pages 523—538
DOI https://doi.org/10.2147/DDDT.S188893
Checked for plagiarism Yes
Review by Single-blind
Peer reviewers approved by Dr Colin Mak
Peer reviewer comments 2
Editor who approved publication: Professor Manfred Ogris
目的:免疫检查点抑制剂发展迅速,并已证实在多种肿瘤中具有抗肿瘤活性。为了评价 atezolizumab 治疗肿瘤的疗效和安全性,我们进行了荟萃分析。
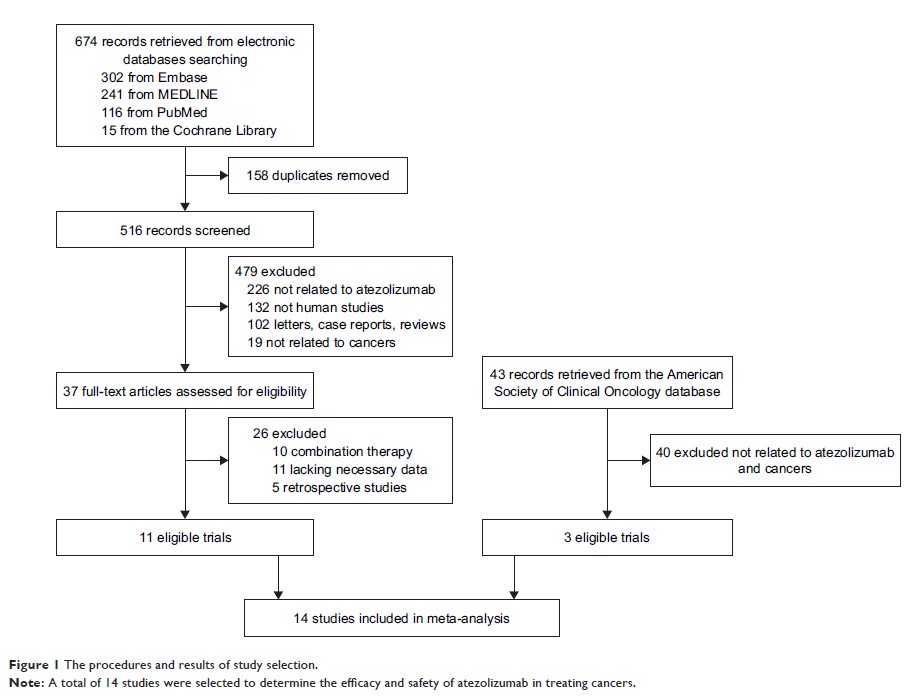
方法:我们检索了 Embase、PubMed、MEDLINE、Cochrane 图书馆和美国临床肿瘤学会数据库。主要观察指标是任何级别不良事件和 3 级及以上的不良事件。次要观察指标是总体客观反应率、6 个月无进展生存率、1 年总生存率、中位无进展生存期和中位总生存期。
结果:我们的荟萃分析基于 14 项临床试验,共纳入 3,266 名患者。任何级别不良事件的总风险达到 69%,而 3 级及以上的不良事件仅有 13%。药物相关死亡率为 0.17%。主要常见不良事件包括疲劳(24.5%)、食欲减退(13.2%)、恶心(12.3%)、腹泻(10.8%)、发热(10.7%)、瘙痒(9.6%)、咳嗽(9.5%)、周围水肿(8.6%)和皮疹(8.4%)。最常见的严重不良事件是疲劳(2.2%)、贫血(1.9%)和呼吸困难(1.9%)。同时,我们发现 6% 的患者达到完全缓解,16% 部分缓解。6 个月无进展生存率和 1 年总生存率分别为 0.36(95% CI:0.31-0.41)和 0.55(95% CI:0.49-0.61)。中位无进展生存期为 1.5-6.1 月,中位总生存期为 5.9-28.9 月。
结论:Atezolizumab 在治疗具有可接受风险的肿瘤方面具有相当大的潜力。
关键词:atezolizumab,安全性,疗效,肿瘤,荟萃分析