114027
论文已发表
注册即可获取德孚的最新动态
IF 收录期刊
- 3.4 Breast Cancer (Dove Med Press)
- 3.2 Clin Epidemiol
- 2.6 Cancer Manag Res
- 2.9 Infect Drug Resist
- 3.7 Clin Interv Aging
- 5.1 Drug Des Dev Ther
- 3.1 Int J Chronic Obstr
- 6.6 Int J Nanomed
- 2.6 Int J Women's Health
- 2.9 Neuropsych Dis Treat
- 2.8 OncoTargets Ther
- 2.0 Patient Prefer Adher
- 2.2 Ther Clin Risk Manag
- 2.5 J Pain Res
- 3.0 Diabet Metab Synd Ob
- 3.2 Psychol Res Behav Ma
- 3.4 Nat Sci Sleep
- 1.8 Pharmgenomics Pers Med
- 2.0 Risk Manag Healthc Policy
- 4.1 J Inflamm Res
- 2.0 Int J Gen Med
- 3.4 J Hepatocell Carcinoma
- 3.0 J Asthma Allergy
- 2.2 Clin Cosmet Investig Dermatol
- 2.4 J Multidiscip Healthc

已发表论文
负载熊果酸的 PVP-PCL 纳米载药微球的体内外抗肝癌的疗效评价
Authors Zhang H, Zheng D, Ding J, Xu H, Li X, Sun W
Published Date March 2015 Volume 2015:10 Pages 1909—1920
DOI http://dx.doi.org/10.2147/IJN.S77125
Received 6 November 2014, Accepted 28 December 2014, Published 11 March 2015
Approved for publication by Dr Lei Yang
目的:探讨采用聚乙烯吡咯烷酮-b-聚己内酯共聚物 (PVP-b-PCL) 合成的熊果酸载药纳米微球抗肝癌的体内外疗效评价,同时对其作用机理进行探讨,并评价 PVP- PCL 作为药物载体的生物相容性。
方法:用开环聚合法制备 PVP-b-PCL 共聚物,采用溶剂分散法制备熊果酸载药纳米微球。测定熊果酸载药纳米微球的相关表征、载药量和包封率以及该微球的体外释放曲线。采用 FITC 荧光标记粒子细胞摄取实验,探讨熊果酸载药纳米微球抗肿瘤作用不同于裸药的机制。以 CCK-8 法及流式细胞分析法,评价该纳米微球在体外对于 H22 肝癌细胞的抗肿瘤效果及凋亡影响,并与熊果酸裸药相比较,以及在该细胞上验证空白微球的毒性。在 ICR 小鼠皮下接种 H22 肿瘤模型,分析熊果酸纳米微球的体内分布,采用腹腔内注射给药,通过影像学等手段验证纳米微球的抗肿瘤活性和副作用,并与熊果酸裸药比较。通过 Western blot 及免疫组化方法研究细胞及组织内相关蛋白水平变化,判断其抗肝癌作用可能的作用机制。
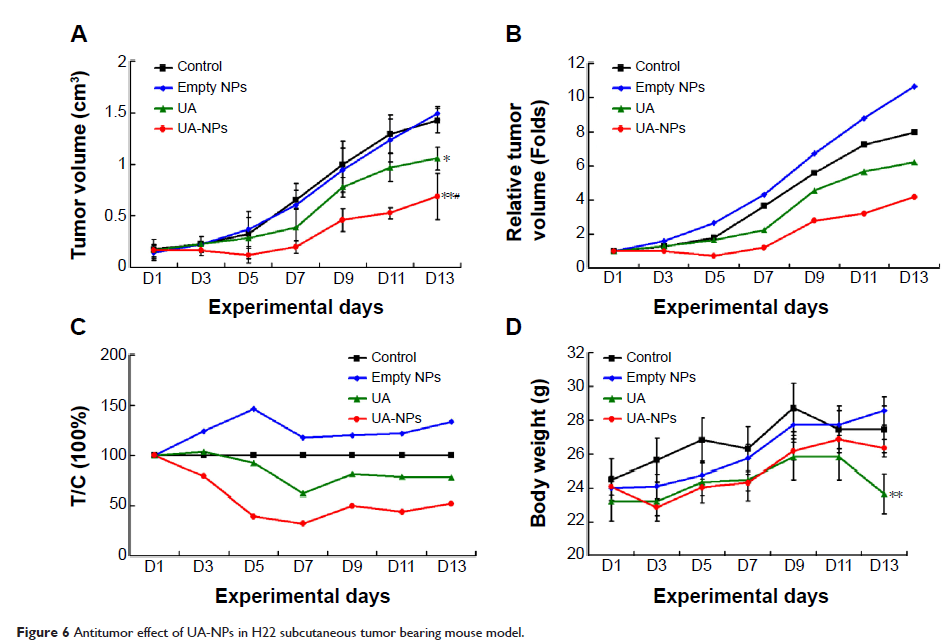
结果:通过对熊果酸载药纳米微球的表征检测,载药微球的平均粒径 120.0±4.0 nm,载药量在 12% 左右,包封率超过 80%。体外释放实验显示,载药微球具有缓释特征,在最初的 12 小时熊果酸释放了近 30%,而随后则表现为一个缓慢释放的特点。荧光标记粒子的细胞摄取实验证实,微球可通过胞吞作用进入细胞,在细胞内释放药物,这是微球不同于裸药的抗肿瘤机制。由细胞生存率曲线可以见到在 H22 细胞上熊果酸微球所造成的细胞杀伤作用明显强于同样浓度的裸药,且呈现了显著的浓度依赖性,而空白微球浓度达 800μg/ml 时,对于肿瘤细胞无明显毒性。流式细胞检测结果显示熊果酸微球在作用 H22 细胞后细胞凋亡率显著高于裸药。通过体内分布实验发现随着时间的延长,纳米载药微球进入肿瘤内的药物浓度逐渐升高,而裸药却与之相反。体内抑瘤实验可以发现熊果酸纳米载药微球较裸药具有更好的抑瘤效果,同时通过 Western blot 及免疫组化方法研究熊果酸纳米载药微球较裸药可以更明显的下调 COX-2、Bcl-2 蛋白表达,上调 Bax 和凋亡相关蛋白 Caspase-3 的表达。
结论:熊果酸对肝癌细胞具有增殖抑制及诱导凋亡作用,其机制可能通过抑制 COX-2 表达及增加凋亡相关蛋白表达有关,且本文中所构建的熊果酸载药纳米微球在体内试验中较裸药具有更好的抗肿瘤效果,载体无毒,具有良好的生物相容性。可见,负载熊果酸的 PVP-PCL 纳米载药微球是抗肝癌药物递送体系发展的新方向,具有良好的实用价值和发展前景。
Keywords: apoptosis, liver cancer, drug delivery, antitumor
方法:用开环聚合法制备 PVP-b-PCL 共聚物,采用溶剂分散法制备熊果酸载药纳米微球。测定熊果酸载药纳米微球的相关表征、载药量和包封率以及该微球的体外释放曲线。采用 FITC 荧光标记粒子细胞摄取实验,探讨熊果酸载药纳米微球抗肿瘤作用不同于裸药的机制。以 CCK-8 法及流式细胞分析法,评价该纳米微球在体外对于 H22 肝癌细胞的抗肿瘤效果及凋亡影响,并与熊果酸裸药相比较,以及在该细胞上验证空白微球的毒性。在 ICR 小鼠皮下接种 H22 肿瘤模型,分析熊果酸纳米微球的体内分布,采用腹腔内注射给药,通过影像学等手段验证纳米微球的抗肿瘤活性和副作用,并与熊果酸裸药比较。通过 Western blot 及免疫组化方法研究细胞及组织内相关蛋白水平变化,判断其抗肝癌作用可能的作用机制。
结果:通过对熊果酸载药纳米微球的表征检测,载药微球的平均粒径 120.0±4.0 nm,载药量在 12% 左右,包封率超过 80%。体外释放实验显示,载药微球具有缓释特征,在最初的 12 小时熊果酸释放了近 30%,而随后则表现为一个缓慢释放的特点。荧光标记粒子的细胞摄取实验证实,微球可通过胞吞作用进入细胞,在细胞内释放药物,这是微球不同于裸药的抗肿瘤机制。由细胞生存率曲线可以见到在 H22 细胞上熊果酸微球所造成的细胞杀伤作用明显强于同样浓度的裸药,且呈现了显著的浓度依赖性,而空白微球浓度达 800μg/ml 时,对于肿瘤细胞无明显毒性。流式细胞检测结果显示熊果酸微球在作用 H22 细胞后细胞凋亡率显著高于裸药。通过体内分布实验发现随着时间的延长,纳米载药微球进入肿瘤内的药物浓度逐渐升高,而裸药却与之相反。体内抑瘤实验可以发现熊果酸纳米载药微球较裸药具有更好的抑瘤效果,同时通过 Western blot 及免疫组化方法研究熊果酸纳米载药微球较裸药可以更明显的下调 COX-2、Bcl-2 蛋白表达,上调 Bax 和凋亡相关蛋白 Caspase-3 的表达。
结论:熊果酸对肝癌细胞具有增殖抑制及诱导凋亡作用,其机制可能通过抑制 COX-2 表达及增加凋亡相关蛋白表达有关,且本文中所构建的熊果酸载药纳米微球在体内试验中较裸药具有更好的抗肿瘤效果,载体无毒,具有良好的生物相容性。可见,负载熊果酸的 PVP-PCL 纳米载药微球是抗肝癌药物递送体系发展的新方向,具有良好的实用价值和发展前景。
Keywords: apoptosis, liver cancer, drug delivery, antitumor