113173
论文已发表
注册即可获取德孚的最新动态
IF 收录期刊
- 3.4 Breast Cancer (Dove Med Press)
- 3.2 Clin Epidemiol
- 2.6 Cancer Manag Res
- 2.9 Infect Drug Resist
- 3.7 Clin Interv Aging
- 5.1 Drug Des Dev Ther
- 3.1 Int J Chronic Obstr
- 6.6 Int J Nanomed
- 2.6 Int J Women's Health
- 2.9 Neuropsych Dis Treat
- 2.8 OncoTargets Ther
- 2.0 Patient Prefer Adher
- 2.2 Ther Clin Risk Manag
- 2.5 J Pain Res
- 3.0 Diabet Metab Synd Ob
- 3.2 Psychol Res Behav Ma
- 3.4 Nat Sci Sleep
- 1.8 Pharmgenomics Pers Med
- 2.0 Risk Manag Healthc Policy
- 4.1 J Inflamm Res
- 2.0 Int J Gen Med
- 3.4 J Hepatocell Carcinoma
- 3.0 J Asthma Allergy
- 2.2 Clin Cosmet Investig Dermatol
- 2.4 J Multidiscip Healthc

MiR-152 通过与 DNMT1 相互作用的抑制鼻咽癌的侵袭、迁移
Authors Lu Z, Du M, Qian L, Zhang N, Gu J, Ding K, Wu J, Zhu H, He X, Yin L
Received 18 October 2017
Accepted for publication 17 January 2018
Published 27 March 2018 Volume 2018:11 Pages 1733—1741
DOI https://doi.org/10.2147/OTT.S154464
Checked for plagiarism Yes
Review by Single-blind
Peer reviewer comments 2
Editor who approved publication: Dr Jianmin Xu
Background: In recent years, miR-152
has been dysregulated in a variety of tumors and used as a tumor suppressor.
Nevertheless, its role in nasopharyngeal carcinoma (NPC) remains unidentified.
材料与方法:实时荧光定量 PCR 被用来分析鼻咽癌细胞株中 miR-152 的表达。 从 GEO 数据库(GSE36682) 获得了 NPC 组织中的 MiR-152 表达谱。通过细胞侵袭,伤口愈合和细胞活力测定来确定 miR-152 对 NPC 细胞的侵袭和增殖的影响。流式细胞术检测细胞凋亡,并进行蛋白质印迹以测量靶基因的表达。焦磷酸测序法检测鼻咽癌细胞甲基化水平。
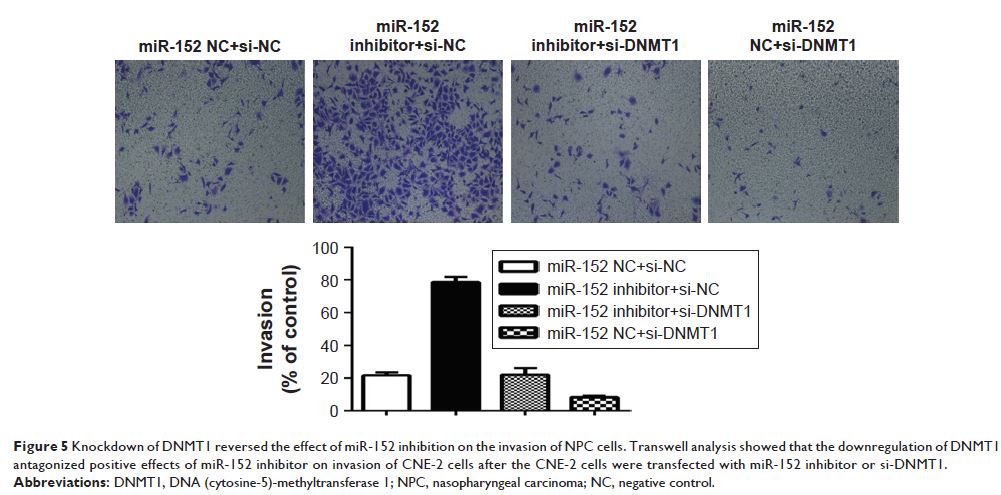
结果:在这项研究中,miR-152 在 NPC 组织和细胞系中下调。当 miR-152 增强时,NPC 细胞的侵袭和迁移受到抑制。然而,miR-152 对 NPC 细胞的增殖没有影响。进行荧光素酶报告基因分析,结果显示 DNMT1 是鼻咽癌细胞中 miR-152 的直接靶点。 DNMT1 下调和 miR-152 过度表达都逆转了 miR-152 抑制对 NPC 细胞的影响。另外,当 DNMT1 表达下调时,miR-152 表达增加是因为抑制 miR-152 的甲基化水平。
结论:miR-152 的过表达通过靶向 DNMT1 抑制鼻咽癌细胞的迁移和侵袭。此外,DNMT1 通过 DNA 甲基化调节 miR-152 的表达。总体而言,新型 miR-152-DNMT1 调控回路可以更好地了解鼻咽癌的发病机制和鼻咽癌新的表观遗传学治疗靶点。
关键词:miR-152,DNMT1,NPC,甲基化