113173
论文已发表
注册即可获取德孚的最新动态
IF 收录期刊
- 3.4 Breast Cancer (Dove Med Press)
- 3.2 Clin Epidemiol
- 2.6 Cancer Manag Res
- 2.9 Infect Drug Resist
- 3.7 Clin Interv Aging
- 5.1 Drug Des Dev Ther
- 3.1 Int J Chronic Obstr
- 6.6 Int J Nanomed
- 2.6 Int J Women's Health
- 2.9 Neuropsych Dis Treat
- 2.8 OncoTargets Ther
- 2.0 Patient Prefer Adher
- 2.2 Ther Clin Risk Manag
- 2.5 J Pain Res
- 3.0 Diabet Metab Synd Ob
- 3.2 Psychol Res Behav Ma
- 3.4 Nat Sci Sleep
- 1.8 Pharmgenomics Pers Med
- 2.0 Risk Manag Healthc Policy
- 4.1 J Inflamm Res
- 2.0 Int J Gen Med
- 3.4 J Hepatocell Carcinoma
- 3.0 J Asthma Allergy
- 2.2 Clin Cosmet Investig Dermatol
- 2.4 J Multidiscip Healthc

通过 “一步自组装” 策略构建基于聚乙烯亚胺的多功能化纳米载体用于基因和化疗药物联合治疗
Authors Jiang D, Wang M, Wang T, Zhang B, Liu C, Zhang N
Received 31 May 2017
Accepted for publication 25 September 2017
Published 6 December 2017 Volume 2017:12 Pages 8681—8698
DOI https://doi.org/10.2147/IJN.S142966
Checked for plagiarism Yes
Review by Single-blind
Peer reviewers approved by Dr Lakshmi Kiran Chelluri
Peer reviewer comments 3
Editor who approved publication: Dr Linlin Sun
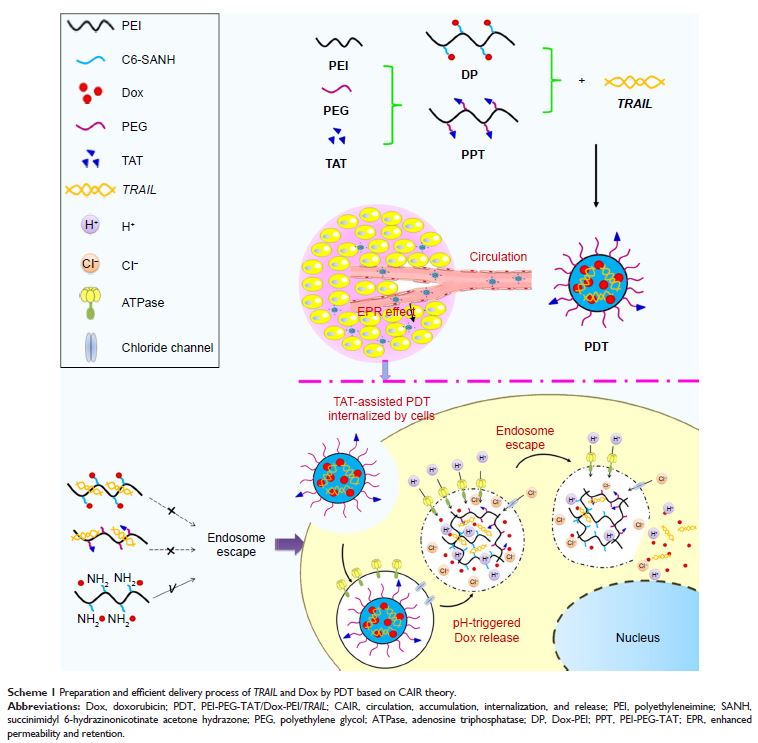
摘要:联合基因疗法和化疗以实现协同抗肿瘤效果是近些年的研究热点之一。在本课题中,我们基于纳米载体在体内的循环、聚集、入胞和释放过程(circulation, accumulation,
internalization, and release,“CAIR”理论)构建人肿瘤坏死因子相关的凋亡诱导配体质粒(TRAIL )和多柔比星(doxorubicin,Dox)共载多功能纳米载体。选择聚乙烯亚胺(polyethyleneimine,PEI)为骨架材料合成聚乙烯亚胺-聚乙二醇-穿膜肽(PEI–polyethylene glycol–TAT,PPT)。通过 C6-琥珀酰亚胺基 6-肼基烟酸酯丙酮腙(C6-succinimidyl
6-hydrazinonicotinate acetone hydrazone,C6-SANH)将 Dox 共价连接到 PEI 上,合成 pH 敏感共价聚合物(Dox-PEI, DP)。用 DP 和 PPT 掺和压缩 TRAIL ,通过 “一步自组装” 策略制备 TRAIL 和 DOX 共载纳米载体 PPT/DP/TRAIL (PDT)。琼脂糖凝胶电泳实验结果表明,PPT、DP 和 C6-SANH-PEI 材料具有相似的基因压缩能力,均能够在质量比为 100:64 时将 TRAIL 完全压缩。选择游离 Dox 和单载 TRAIL 纳米载体(PPT/C6-SANH-PEI/TRAIL ,PCT)作为对照组验证 PDT 的协同抗肿瘤效果。体外蛋白印迹实验结果表明,与游离 TRAIL 相比,PDT 和 PCT 均可上调 TRAIL 蛋白的表达。体外细胞毒实验结果表明,与游离 DOX 和 PCT 相比,PDT 的体外细胞杀伤作用显著提高(P <0.01)。此外,选择鼠源的 TRAIL 质粒构建鼠源 TRAIL 和 Dox 共载纳米载体 PDT,体内抗肿瘤实验结果表明与游离 Dox 和鼠源 PCT 相比,鼠源 PDT 具有更好的抗肿瘤效果(P <0.05)。综上,本课题构建的 TRAIL 和 Dox 共载纳米载体 PDT 可用来实现 TRAIL 和 Dox 的协同抗肿瘤效果,该载体为促进癌症的基因-药物联合治疗提供了可能。
关键词:多功能;基因治疗;化疗;TRAIL ;一步自组装;“CAIR”理论